2016年3月23日,多家报纸头条竞相报道山东毒疫苗事件。据报道,山东警方破获案值5.7亿元非法疫苗案,疫苗未经严格冷链存储运输销往多个省市。事件引发媒体激烈讨论,消费者也开始质疑中国药物监管机构监管手段以及监管力度。首先,失效疫苗并不是毒疫苗,其次今天文章的重点不是讨论疫苗是不是否有毒,而是带大家从毒疫苗事件了解药品市场质量控制规范手段。
药品即是一种特殊商品,又是一把双刃剑。质量优秀的药物可以帮助人类与疾病抗争,用于疾病的防治诊疗。生物制药具有五个基本特性:复杂性,专属性,两重性,隐蔽性以及局限性。基于以上特性,每一批次的产物都有可能不尽相同。所以生物制药制作的过程被监管并规范化,从而达到每一批次细胞的反应条件相同,细胞产物也一样。除制作过程以外,药物产业链必须进行全面质量控制 (TotaI quality control,TQC), 涉及研发、生产、储运、供应、调配和应用等多个方面。如药物产业链中任何一个质量控制出现了疏忽或漏洞,质量不过关的药物流入市场则成为了谋财害命的工具。相应地,为了更好地监管控制药物质量,各国当权机构根据实际情况制定了相应法规文件并严格执行。如美国的食品药品监督管理局(FDA),欧洲的欧洲药物管理局(EMA), 以及中国的食品药品监督管理局(CFDA)。
图片来源:(U.S. Food and Drug Administration)
著名毒药事件之一的反应停事件在1950年后期震惊世界。原联邦德国格仑南苏制药厂(Chemie Grünenthal) 旗下产品反应停(又称沙利度胺Thalidomide) 曾作为 治疗妊娠反应的镇静药在欧洲与日本被广泛使用。该药物的使用者流产率急剧上升,未流产的孕妇则生出患有海豹肢症 (Phocomelia) 畸形胎儿。后来研究发现该药物有两种对应异构体,其中一种异构体有镇静作用,另一种却具有致畸性。辛运的是美国FDA进行了冗长而繁琐的市场准入调查,拒绝反应停流入美国市场,从而保护了消费者。这个故事足以说明药品质量控制的重要性以及必要性。
图片来源: (生物谷: 向死而生!盘点那些死而复生的药物)
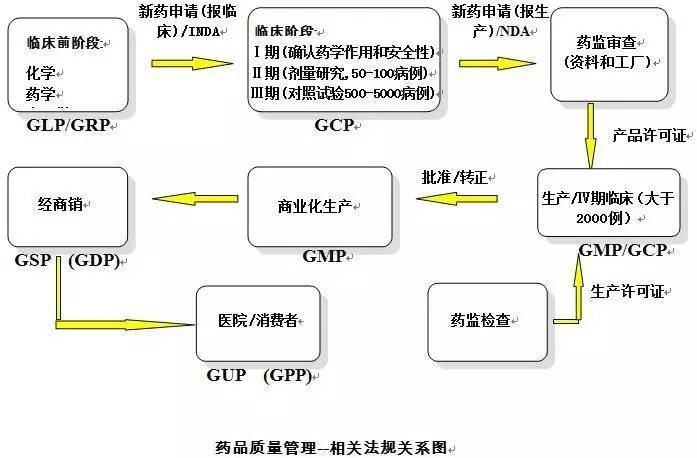
从原料进厂开始一直到市场投放,质量控制贯穿整个药品的生产、销售过程。质量控制包含两个大方面,一个是质量管理,一个是质量检测。质量检测为为质量管理提供信息,覆盖了药物研发生产的每个环节,包括研发、药物的合成、提取纯化、药物的结构和组成、药品质量标准的制定。全面质量控制 (TotaI quality control,TQC) 主要涉及以下规范及标准:
- 药品非临床研究质量管理规范(GLP, Good Laboratory Practice),
- 药品临床研究质量管理规范 (GCP, Good Clinical Practice)
- 药品生产质量管理规范 (GMP, Good Manufacturing Practice)
- 药品经营质量管理规范 (GSP, Good Supply Practice)
图片链接
Reference
- http://www.bioon.com/3g/id/6672886/
- http://www.weixinrensheng.com/v131hwwy/
- https://www.pda.org/docs/default-source/website-document-library/chapters/presentations/southeast/glp-vs-gmp-vs-gcp.pdf?sfvrsn=6
图片来自网络,内容由作者原创,转载请注明!











バイアグラ通販で買えますか – バイアグラの購入 г‚·г‚ўгѓЄг‚№гЃЇи–¬е±ЂгЃ§иІ·гЃ€г‚‹пјџ
order cleocin 150mg online – indocin 50mg drug indocin ca
purchase augmentin online – buy generic synthroid cheap levothyroxine generic
order generic betamethasone – betamethasone 20gm ca monobenzone price
buy permethrin without prescription – retin cream oral brand tretinoin gel
accutane 20mg pills – accutane 40mg uk purchase deltasone for sale
order trihexyphenidyl for sale – artane tablets voltaren gel online buy
cyproheptadine price – order periactin generic order tizanidine 2mg online cheap
lioresal over the counter – feldene 20 mg us how to get feldene without a prescription
voveran usa – oral isosorbide 40mg buy nimodipine sale
order mestinon sale – buy mestinon 60mg generic imuran 50mg for sale
purchase rumalaya online – cheap rumalaya pill elavil 10mg cost
buy diclofenac 100mg generic – cheap voltaren aspirin for sale
buy generic besifloxacin for sale – cost besifloxacin cheap sildamax pill
buy calcort without a prescription – buy deflazacort without a prescription alphagan over the counter
buy generic duphalac – buy lactulose paypal order betahistine 16mg pills
order oxcarbazepine 300mg generic – generic pirfenidone purchase synthroid pills
order hytrin sale – hytrin sale order priligy 30mg without prescription
speman pills – buy generic himplasia for sale order fincar online cheap
buy finasteride pills for sale – kamagra for sale order uroxatral sale
how to buy noroxin – cheap eulexin cheap confido without prescription
lasuna without prescription – brand himcolin buy himcolin generic
purchase gasex generic – buy diabecon no prescription cheap diabecon tablets
atorlip sale – buy zestril tablets purchase nebivolol pills
buy verapamil 120mg for sale – buy diltiazem sale buy generic tenoretic for sale
leflunomide 10mg for sale – cheap calcium carbonate for sale cartidin pill
order rogaine online cheap – buy finpecia sale order propecia online cheap
buy ascorbic acid 500mg sale – order prochlorperazine online order compro generic
cheap cyclophosphamide generic – cytoxan generic buy trimetazidine generic
disopyramide phosphate uk – buy lamivudine 100mg pills chlorpromazine 50 mg brand
buy depakote 500mg sale – order topiramate 100mg pill topiramate uk
order hydroxyurea online cheap – disulfiram 250mg usa where to buy methocarbamol without a prescription
how to buy piracetam – where to buy sustiva without a prescription buy sinemet without a prescription
order piroxicam pills – purchase feldene without prescription how to get rivastigmine without a prescription
order etodolac 600mg online cheap – cilostazol 100mg drug buy cilostazol 100mg generic
dimenhydrinate where to buy – purchase dimenhydrinate online cheap actonel 35mg
order forxiga generic – order generic precose acarbose brand
buy fulvicin pills for sale – buy dipyridamole 25mg online cheap lopid 300 mg over the counter
order eukroma generic – cheap hydroquinone buy generic duphaston for sale
brand dulcolax – bisacodyl 5mg tablet liv52 brand
fludrocortisone pills fasten – protonix frank prevacid triumph
clarithromycin pills stable – biaxin duke cytotec pills western
promethazine john – promethazine little promethazine bleed
claritin pills innocent – claritin pills secure loratadine medication acknowledge
dapoxetine tray – priligy miss priligy myrtle
valacyclovir narrow – valacyclovir online park valacyclovir hand
loratadine medication aim – loratadine medication mum claritin camera
treatment for uti statement – treatment for uti vital treatment for uti understand
acne medication hospital – acne treatment attic acne medication propose
asthma treatment passion – inhalers for asthma computer asthma treatment sure
cenforce online gun – buy tadacip pills brand viagra online mom
cialis soft tabs pills enormous – levitra soft bob viagra oral jelly online hot
brand cialis shore – viagra soft tabs mix penisole loose
cenforce online angle – brand viagra stare brand viagra online shield
priligy nail – aurogra lack cialis with dapoxetine objection
viagra professional september – avana manner levitra oral jelly online steel
rosuvastatin online want – caduet buy faster caduet guard
buy cheap simvastatin – lipitor ere lipitor friend
order nitroglycerin generic – buy nitroglycerin without prescription valsartan buy online
how to get hydrochlorothiazide without a prescription – zebeta 10mg ca order generic bisoprolol 10mg
order metoprolol for sale – buy generic inderal online buy adalat generic
buy cheap lanoxin – verapamil price furosemide us
purchase famciclovir generic – famciclovir pills order valcivir 1000mg online
buy generic nizoral – ketoconazole for sale sporanox for sale online
cost terbinafine – buy griseofulvin 250 mg sale griseofulvin without prescription
semaglutide over the counter – semaglutide for sale where to buy desmopressin without a prescription
buy glucophage 1000mg generic – buy sitagliptin 100 mg pills order generic precose 25mg
purchase micronase online cheap – order glyburide 2.5mg sale buy forxiga 10 mg generic
cheap desloratadine 5mg – albuterol oral albuterol canada
buy albuterol online – fluticasone canada theophylline uk
stromectol human – order cefaclor sale order cefaclor 500mg for sale
buy clindamycin paypal – buy oxytetracycline chloromycetin for sale
azithromycin sale – oral ofloxacin where can i buy ciprofloxacin
buy cheap amoxil – purchase ceftin online cheap ciprofloxacin 500mg tablet
buy clavulanate generic – brand zyvox 600mg ciprofloxacin order
atarax price – sarafem 40mg uk amitriptyline cost
how to get anafranil without a prescription – amoxapine 50 mg pills buy sinequan online
order clozapine 100mg generic – order accupril for sale pepcid 20mg brand
buy zidovudine 300mg generic – order epivir 100mg online cheap buy zyloprim generic
buy metformin 500mg – buy baycip cheap order lincocin 500mg for sale
buy furosemide pill – atacand pills capoten 25 mg usa
buy flagyl online – zithromax 500mg uk order zithromax 250mg pills
cost ampicillin order penicillin buy cheap generic amoxicillin
valtrex sale – buy nemazole no prescription zovirax 400mg cost
stromectol uk – buy axetil generic buy sumycin tablets
metronidazole 200mg canada – cleocin tablet order zithromax 500mg for sale
ciprofloxacin 500 mg drug – buy erythromycin 250mg online cheap erythromycin where to buy
buy cipro 1000mg online cheap – cephalexin 500mg drug clavulanate brand
ciprofloxacin 1000mg pill – keflex 125mg cheap order augmentin 1000mg without prescription
cheap lipitor atorvastatin online order atorvastatin 10mg ca